全新三代长效升白针——艾贝格司亭α获批上市,助力患者顺利渡过化疗难关
2023年5月9日,全球首个第三代双分子升白针艾贝格司亭α注射液获批上市,用于成年非髓性恶性肿瘤患者在接受容易引起发热性中性粒细胞减少症的骨髓抑制性抗癌药物治疗时,降低以发热性中性粒细胞减少症为表现的感染发生率。
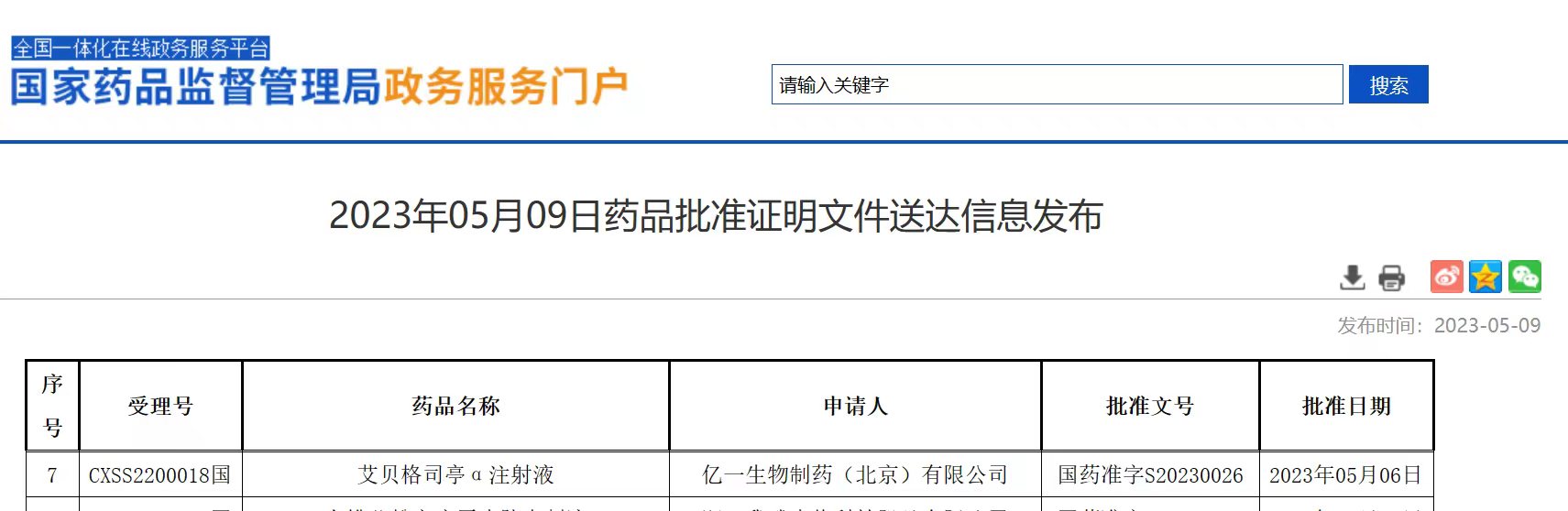
艾贝格司亭α是一种长效升白针,在每次化疗结束48小时后皮下注射,每个化疗周期只需注射一次。艾贝格司亭α的上市,为化疗患者的减负带来了新希望,助力肿瘤患者顺畅渡过化疗难关。
艾贝格司亭α,为化疗患者的治疗减负
化疗可以说是肿瘤治疗的基石疗法,但很多肿瘤患者对化疗的副作用十分恐惧,常有“化疗化疗,一化就了”的说法,中性粒细胞减少就是化疗十分常见的副作用之一。据统计,25%~40%化疗初治患者会出现中性粒细胞减少;而因中性粒细胞减少导致化疗延迟和减量的患者超过60%;需要重视的是,化疗过程中发生剂量改变的患者有超过60%会再次出现中性粒细胞减少[1]。而且根据美国的统计数据,大约5.2%的癌症相关住院治疗与中性粒细胞减少有关,其中2.6%~7.4%的癌症患者会因此离世[2]。
所以,在化疗过程中预防中性粒细胞减少的发生,有助于帮助患者的化疗减负,取得更好的癌症治疗效果,新一代长效升白针艾贝格司亭α可更有效地做到这一点。
艾贝格司亭α是国内首个采用Fc融合技术的G-CSF药物,抛弃了传统长效升白针的聚乙二醇(PEG)化技术路线,每一个Fc片段融合了两个G-CSF分子,可以促进G-CSFR的二聚化,激活下游信号通路,发挥升白作用。另外,艾贝格司亭α抛弃PEG化路线,也使得PEG包裹影响G-CSF和受体结合的问题不复存在,表现出良好的药效学活性。
艾贝格司亭α也是目前唯一与短效G-CSF和传统长效G-CSF都做过大样本头对头临床研究的G-CSF药物。临床研究结果显示,第3化疗周期中,艾贝格司亭α在3级和4级中性粒细胞减少症的发生率上,均显著低于短效G-CSF药物[3];而与其他长效G-CSF药物相比,在第4化疗周期中,艾贝格司亭α的重度中性粒细胞减少发生率显著低于其他长效G-CSF药物[4]。
艾贝格司亭α,为化疗患者的身体减负
艾贝格司亭α和PEG化的G-CSF药物,都属于长效升白药,那他们之间有什么区别呢?
前面提到了艾贝格司亭α抛弃了传统的PEG化技术路线,这样做的原因是什么呢?
短效升白针的有效成分是G-CSF,但是作用时间短,需要每天注射,给患者带来更多的创伤和不便。为解决这些问题,第二代升白针使用PEG来修饰G-CSF,显著延长了半衰期,每个化疗周期只需要注射一次,但给患者带来了方便的同时,也带来了新的问题,比如安全性问题。
其实,PEG化修饰本身是有助于降低药物蛋白致敏性的,但由于现代生活中很多日用品如牙膏、洗发液都含有PEG,多数人体内已产生PEG抗体,这就导致PEG本身成为了一个致敏原[5]。
在新冠病毒流行期间,PEG被用作部分新冠疫苗的赋形剂,一些疫苗过敏反应就被认为和PEG相关[6]。而采用PEG化技术的G-CSF药物,被发现部分血管炎、荨麻疹等一系列过敏反应同样与PEG相关,过敏反应的发生率在1.38%左右[7,8],并有发生严重过敏反应的案例报道[9]。
因此,抛弃了PEG化路线的艾贝格司亭α不易致敏,更加安全,能够为化疗患者的身体减负。
随着艾贝格司亭α在国内的获批,这一最新的G-CSF药物,为化疗患者的治疗减负带来了新希望,进一步助力肿瘤患者顺畅渡过化疗难关,让我们共同期待艾贝格司亭α能造福更多的癌症患者!
参考文献:
1.Lalami Y, Klastersky J. Impact of chemotherapy-induced neutropenia (CIN) and febrile neutropenia (FN) on cancer treatment outcomes: an overview about well-established and recently emerging clinical data[J]. Critical reviews in oncology/hematology, 2017, 120: 163-179..2.Snegovoy A, Kononenko I, Chernova A, et al. Incidence of severe and febrile neutropenia in cancer patients treated with myelosuppressive chemotherapy in real clinical oncology practice: Preliminary results from the FLAME study[J]. 2022.3.Daley W, Shao Z, Zhang Q, et al. Abstract P5-16-14: A randomized, multicenter phase III study of once-per-cycle administration of efbemalenograstim alfa (F-627), a novel long-acting dimeric rhG-CSF, for prophylaxis of chemotherapy-induced neutropenia in patients with breast cancer[J]. Cancer Research, 2022, 82(4_Supplement): P5-16-14-P5-16-14.4.Glaspy J, Daley W, Bondarenko I, et al. A Phase III, Randomized, Multi-Center, Open-Label, Fixed Dose, Neulasta Active-Controlled Clinical Trial of F-627, a Novel G-CSF, in Women with Breast Cancer Receiving Myelotoxic Chemotherapy[J]. Blood, 2021, 138: 4290.5.Yang Q, Jacobs T M, McCallen J D, et al. Analysis of pre-existing IgG and IgM antibodies against polyethylene glycol (PEG) in the general population[J]. Analytical chemistry, 2016, 88(23): 11804-11812.6.Lang D M, Patadia D D. Anaphylaxis to vaccinations: a review of the literature and evaluation of the COVID 19 mRNA vaccinations[J]. Cleve Clin J Med, 2021.7.Neumann T A, Foote M A. The safety profile of filgrastim and pegfilgrastim[J]. Twenty Years of G-CSF: Clinical and Nonclinical Discoveries, 2012: 395-408.8.Jenabian A, Ehsanpour A, Mortazavizadeh S M R, et al. Evaluating the safety and effectiveness of PegaGen®(pegfilgrastim) for the prevention of chemotherapy-induced febrile neutropenia: a post-marketing surveillance study[J]. Supportive Care in Cancer, 2022, 30(10): 8151-8158.9.Seto Y, Kittaka N, Taniguchi A, et al. Pegfilgrastim-induced vasculitis of the subclavian and basilar artery complicated by subarachnoid hemorrhage in a breast cancer patient: a case report and review of the literature[J]. Surgical Case Reports, 2022, 8(1): 155.